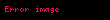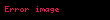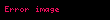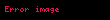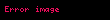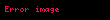Bir sürecin spontaneliği, bir reaksiyonun Gibbs serbest enerjisi değeri nedeniyle, bir enerji girişi olmadan meydana gelip gelmeyeceğini ifade eder.
Gibbs serbest enerjisi şu şekilde verilir:
= Gibbs serbest enerjisi
= entalpi değişimi
= sıcaklık (Kelvin cinsinden)
= entropi değişimi
Gibbs serbest enerji değişimi 0 veya negatif ise, reaksiyonun kendiliğinden olduğu ve sisteme bir enerji girişi olmadan gerçekleşebileceği ifade edilir. Gibbs serbest enerjisi 0'ın üzerinde ise, reaksiyon kendiliğinden olmaz ve ilerlemesi için bir enerji girişi gerekir.
Denge reaksiyonlarında, bir reaksiyonun bir yönü kendiliğinden olurken, ters reaksiyon kendiliğinden olmayacaktır. Bu nedenle, denge için genel bir formül kullanarak:
Eğer 'dan ve oluşumu spontane ise, ve 'den oluşumu spontane olmayacaktır.
Spontane bir sürece örnek, elmasın grafite dönüştürülmesidir, çünkü grafit daha termodinamik olarak kararlı bir yapıya sahiptir. Spontane olmayan bir sürecin bir örneği ise sistemin dışından bir enerji girişi gerektirdiğinden, karbondioksit ve su oluşturmak için metanın oksijende yanması olabilir.
Kaynakça
wikipedia, wiki, viki, vikipedia, oku, kitap, kütüphane, kütübhane, ara, ara bul, bul, herşey, ne arasanız burada,hikayeler, makale, kitaplar, öğren, wiki, bilgi, tarih, yukle, izle, telefon için, turk, türk, türkçe, turkce, nasıl yapılır, ne demek, nasıl, yapmak, yapılır, indir, ücretsiz, ücretsiz indir, bedava, bedava indir, mp3, video, mp4, 3gp, jpg, jpeg, gif, png, resim, müzik, şarkı, film, film, oyun, oyunlar, mobil, cep telefonu, telefon, android, ios, apple, samsung, iphone, xiomi, xiaomi, redmi, honor, oppo, nokia, sonya, mi, pc, web, computer, bilgisayar
Bir surecin spontaneligi bir reaksiyonun Gibbs serbest enerjisi degeri nedeniyle bir enerji girisi olmadan meydana gelip gelmeyecegini ifade eder Gibbs serbest enerjisi su sekilde verilir DG DH TDS displaystyle Delta G Delta H T Delta S DG displaystyle Delta G Gibbs serbest enerjisi DH displaystyle Delta H entalpi degisimi T displaystyle T sicaklik Kelvin cinsinden DS displaystyle Delta S entropi degisimi Gibbs serbest enerji degisimi 0 veya negatif ise reaksiyonun kendiliginden oldugu ve sisteme bir enerji girisi olmadan gerceklesebilecegi ifade edilir Gibbs serbest enerjisi 0 in uzerinde ise reaksiyon kendiliginden olmaz ve ilerlemesi icin bir enerji girisi gerekir Denge reaksiyonlarinda bir reaksiyonun bir yonu kendiliginden olurken ters reaksiyon kendiliginden olmayacaktir Bu nedenle denge icin genel bir formul kullanarak A B C displaystyle ce A lt gt B C Eger A displaystyle A dan B displaystyle B ve C displaystyle C olusumu spontane ise B displaystyle B ve C displaystyle C den A displaystyle A olusumu spontane olmayacaktir Spontane bir surece ornek elmasin grafite donusturulmesidir cunku grafit daha termodinamik olarak kararli bir yapiya sahiptir Spontane olmayan bir surecin bir ornegi ise sistemin disindan bir enerji girisi gerektirdiginden karbondioksit ve su olusturmak icin metanin oksijende yanmasi olabilir Kaynakca 5 Ocak 2019 tarihinde kaynagindan arsivlendi Erisim tarihi 7 Agustos 2019 7 Eylul 2015 tarihinde kaynagindan arsivlendi Erisim tarihi 7 Agustos 2019
 Azərbaycanca
Azərbaycanca Deutsch
Deutsch 日本語
日本語 Lietuvos
Lietuvos සිංහල
සිංහල Türkçe
Türkçe Українська
Українська United State
United State